前沿 | 杨莉莉团队从造血干/祖细胞生成新型细胞用于癌症免疫治疗-pg电子官方
car-t细胞疗法,是一种革命性的免疫疗法,通过基因编辑患者的t细胞,使其具有更强的识别和攻击癌细胞的能力。然而,尽管car-t细胞疗法在治疗某些血液肿瘤方面取得了显著的成功,但其临床潜力仍受到多方面的限制。
首先,car-t细胞疗法的自体特性限制了其在临床应用中的广泛应用。制造car-t细胞的过程复杂且昂贵,同时患者选择也是一个重要的问题。特别是在治疗实体肿瘤方面,car-t细胞的疗效并不尽如人意。
此外,移植物抗宿主病(gvhd)是car-t细胞疗法面临的另一个严重挑战。gvhd是一种严重的并发症,发生在接受异基因免疫细胞治疗的患者身上。在这种情况下,治疗细胞攻击患者自身的健康组织,可能导致严重的器官损伤甚至危及患者的生命。因此,尽管car-t细胞疗法在某些情况下取得了突破性的进展,但其临床应用仍面临着许多挑战,包括制造、成本、患者选择以及治疗后的不良反应等方面。
2024年5月14日,加州大学洛杉矶分校(ucla)杨莉莉团队在 nature 子刊 nature biotechnology 上发表了题为:generation of allogeneic car-nkt cells from hematopoietic stem and progenitor cells using a clinically guided culture method 的研究论文。
该论文描述了一种临床指导的方法,利用造血干/祖细胞(hspc)基因编辑技术和体外无饲养层细胞培养技术,生成用于癌症免疫疗法的“通用型car-nkt”细胞,对多种肿瘤展现强大的抗肿瘤效能。

在这项研究中,研究团队引入了一种体外无饲养层细胞培养方法,将基因改造后的造血干/祖细胞分化为带有嵌合抗原受体(car)的同种异体自然杀伤t细胞(allocar-nkt细胞)。allocar-nkt细胞产量高、纯度高、稳定性强。这些细胞在体内展现了强大的抗肿瘤效能,表现出有效的肿瘤定位、扩增和持久性。
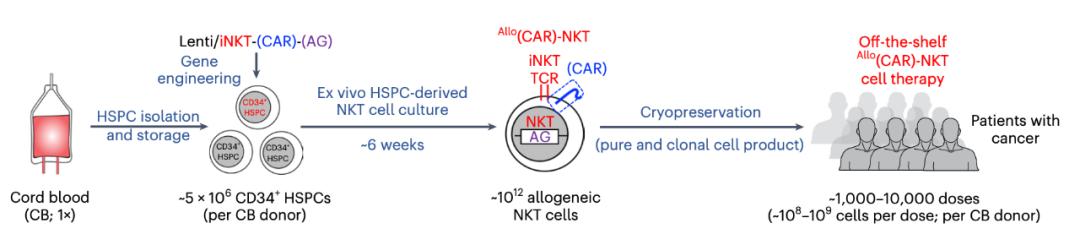
生产allocar-nkt细胞示意图
研究团队生成了针对七种癌症的allocar-nkt细胞,并在多发性骨髓瘤模型中证明了它们的抗肿瘤效力、扩增和持久性。值得关注的是,allocar-nkt细胞能通过选择性消耗免疫抑制的肿瘤相关巨噬细胞(tam)和髓系抑制细胞(mdsc)来改变肿瘤微环境(tme),并有效利用car/tcr/nkr三重靶向机制来对抗肿瘤免疫逃逸。allocar-nkt细胞同样展现出高安全性,以及低移植物抗宿主病(gvhd)和细胞因子释放综合征(crs)风险的特性,并展现出一种稳定的“低免疫原性”表型。
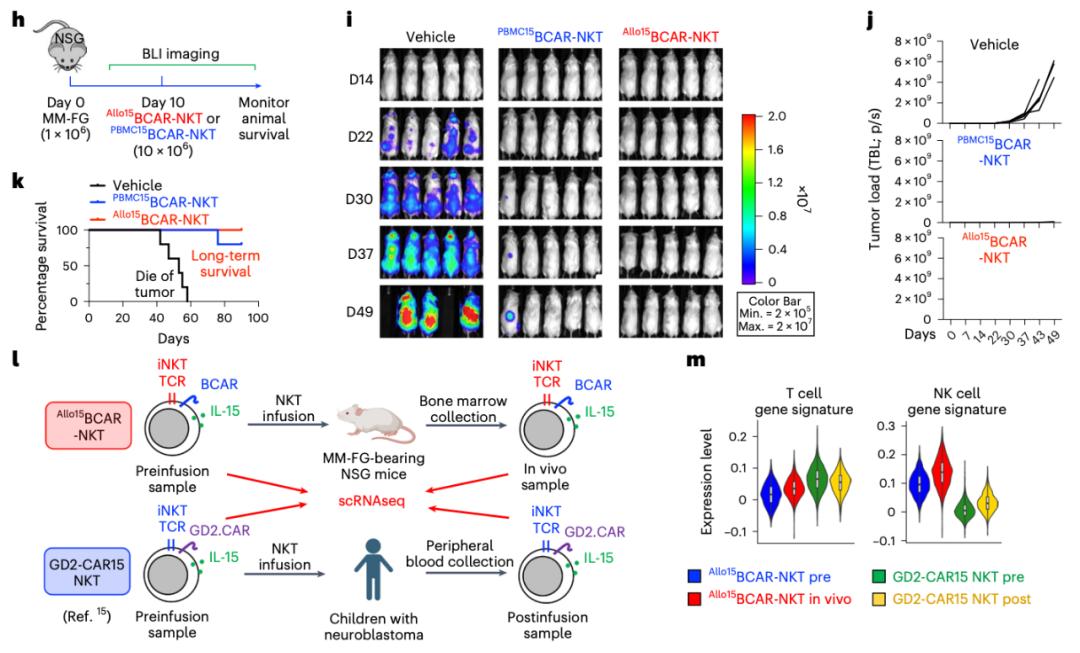
allocar-nkt细胞表现出与pbmc来源的car-nkt细胞相似的抗肿瘤能力,但具有更高的nk细胞属性
与传统的car-t细胞疗法相比,allocar-nkt细胞的显著细胞毒性、效应功能、扩增性使其打破了许多现有疗法的限制。进一步评估allocar-nkt细胞用于通用型癌症免疫疗法的潜力仍需广泛的临床研究。
ucla yang免疫工程实验室(yang engineering immunity lab)致力于研究解码控制肿瘤免疫的细胞和分子机制,并开发新一代肿瘤免疫疗法。杨莉莉教授为该论文通讯作者,课题组博士后李闫瑞德,已毕业博士生周阳及已毕业博士生虞家霁为该论文共同第一作者。(来源:)
论文链接:
https://www.nature.com/articles/s41587-024-02226-y